Notre revue systématique avec méta-analyse sur le risque de méningiomes intracrâniens associé aux médicaments progestatifs, menée en partenariat avec le GHU PARIS, service de neurochirurgie du Pr Johan Pallud.
En analysant 78 études internationales, nous montrons :
– un surrisque majeur avec l’acétate de cyprotérone (estimé à 12,4)
– un surrisque avec l’acétate de médroxyprogestérone
– des signaux pour d’autres macroprogestatifs (acétate de chlormadinone, acétate de nomegestrol, promegestone, medrogestone, desogestrel)
– Un risque accru de méningiomes malins pour certaines molécules
– Une prédominance des localisations à la base du crâne
– Une régression possible mais non systématique de la taille du méningiome après k’arrêt du traitement
Le niveau de preuve varie selon les molécules, mais ces données renforcent la nécessité d’informer clairement les patientes, de limiter les prescriptions (indication strictement nécessaire, dose minimale, durée minimale) et d’assurer un suivi adapté en cas d’exposition prolongée.
Etude à lire ici : https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(26)00038-6/fulltext
Merci à Benoit Hudelist et à toute l’équipe de neurochirurgie du GHU Paris Psychiatrie et Neuroscience – Sainte-Anne pour ce travail collaboratif.
Résumé
Contexte. Les méningiomes sont les tumeurs primitives intracrâniennes les plus fréquentes chez l’adulte. Un lien potentiel entre l’exposition aux progestatifs et la survenue de méningiomes intracrâniens suscite des préoccupations. Nous avons évalué l’association entre différents progestatifs et le risque de méningiome intracrânien, ainsi que des critères secondaires (malignité, localisation, régression).
Méthodes. Nous avons mené une revue systématique et une méta-analyse des études épidémiologiques (anglais/français) rapportant une association entre exposition à un progestatif et méningiome intracrânien. Les bases PubMed/MEDLINE, Embase, Cochrane Library et EPI-PHARE ont été interrogées depuis l’origine jusqu’au 1er novembre 2025, complétées par les rapports de pharmacovigilance et une recherche par références. Ont été exclus : travaux non originaux, résumés sans texte intégral, et études sans exposition éligible ou sans critère de jugement pertinent. Le risque de biais a été évalué par l’échelle de Newcastle-Ottawa et la certitude des preuves par GRADE. Des modèles à effets aléatoires ont été utilisés ; l’hétérogénéité a été estimée par I² ; une synthèse narrative a complété l’analyse.
Résultats. Parmi 542 références dépistées, 78 études ont été incluses dans la revue et 14 études observationnelles de haute qualité dans la méta-analyse. L’acétate de cyprotérone (CPA) était fortement associé à une augmentation du risque de méningiome (5 études ; 1047 cas exposés ; OR combiné 12,36 (IC95 % 7,47-20,45) ; I² 73,8 % ; GRADE modéré). L’acétate de médroxyprogestérone dépôt était également associé (6 études ; 842 cas exposés ; OR 2,68 (1,72-4,19) ; I² 92,7 % ; GRADE faible). Des signaux de risque accru étaient rapportés pour l’acétate de chlormadinone, l’acétate de nomégestrol, la promégestone, la médrogestone et le désogestrel. Une régression après arrêt était décrite pour le CPA et le nomégestrol. Les tumeurs étaient majoritairement situées à la base du crâne antérieure/moyenne, et les formes malignes semblaient plus fréquentes avec le CPA, la chlormadinone et le nomégestrol.
Interprétation. Malgré des limites liées au caractère observationnel, à une confusion résiduelle, à l’hétérogénéité et à l’imprécision pour certaines expositions, certains progestatifs, en particulier les macroprogestatifs à fortes doses, pourraient augmenter le risque de méningiome intracrânien. Une information claire des patients et un suivi clinique, et radiologique si indiqué, sont essentiels.
Données disponibles avant cette étude
Avant d’entreprendre cette étude, nous avons effectué des recherches dans PubMed/MEDLINE, Embase et la Cochrane Database of Systematic Reviews depuis la création des bases de données jusqu’au 1er novembre 2025 (sans restriction linguistique) afin d’identifier les revues systématiques et les méta-analyses antérieures sur les progestatifs systémiques et le risque de méningiome intracrânien. Nous avons également examiné les listes de références des revues éligibles et des documents clés de pharmacovigilance/réglementation (par exemple, EMA, ANSM/EPI-PHARE). Les termes de recherche combinaient « méningiome » avec « progestatif/progestatif ». Nous avons inclus les synthèses de données probantes avec des critères d’éligibilité explicites et une évaluation structurée du risque de biais, et avons exclu les revues narratives et les rapports/séries de cas. Nous avons identifié une revue systématique/méta-analyse antérieure axée sur l’acétate de cyprotérone, rapportant une estimation combinée imprécise (RR : 3,78, IC à 95 % : 0,31-46,39) et jugée comme présentant un risque de biais modéré à élevé ; la certitude était faible. Aucune synthèse antérieure n’a évalué de manière exhaustive d’autres progestatifs ou des résultats tels que la régression tumorale, le risque de malignité ou la prédilection pour la base du crâne.
Valeur ajoutée de cette étude
Cette revue systématique et cette méta-analyse synthétisent la plus grande base de données factuelles contemporaines sur les macro- et microprogestatifs dans diverses populations. Elle identifie des agents spécifiques associés à un risque accru de méningiome et confirme un effet de classe pour les macroprogestatifs. Elle met également en évidence le désogestrel comme un microprogestatif associé au méningiome lors d’une utilisation prolongée. Au-delà de l’incidence, nous documentons une régression ou une stabilisation radiologique constante après l’arrêt du traitement, quantifions le risque élevé de méningiome malin (grade 3 de l’OMS) pour certains agents et délimitons une prédilection pour les emplacements antérieurs et médians de la base du crâne, des résultats directement pertinents pour le dépistage et la prise en charge. Dans l’ensemble, cette étude consolide les connaissances actuelles et fournit une base solide pour orienter la pratique clinique, les politiques et les recherches futures.
Implications de toutes les données disponibles
Compte tenu de l’utilisation répandue et souvent prolongée des progestatifs à des fins contraceptives, pour traiter l’endométriose, dans le cadre d’un traitement ménopausique et pour supprimer les androgènes, les cliniciens devraient systématiquement documenter l’exposition aux progestatifs chez les patientes atteintes ou suspectées d’être atteintes d’un méningiome, envisager l’arrêt des agents à haut risque lorsque cela est possible et envisager un suivi par IRM conformément aux recommandations nationales et aux profils de risque individuels, en particulier chez les femmes exposées de manière prolongée à des doses élevées de macroprogestatifs ou atteintes ou suspectées d’être atteintes d’un méningiome. Toutefois, l’interprétation doit tenir compte de certaines limites importantes : la plupart des données disponibles sont observationnelles, les définitions de l’exposition et les seuils de dose varient d’une étude à l’autre, l’hétérogénéité est importante pour certaines estimations groupées, et les facteurs de confusion résiduels et les biais de surveillance (détection) peuvent gonfler les estimations des risques, en particulier dans les contextes où le dépistage par IRM est structuré. Les preuves concernant plusieurs agents restent limitées et imprécises, et leur généralisation aux hommes et aux populations transgenres est incertaine en raison de rapports incomplets sur le sexe/genre. Les prescripteurs et les régulateurs doivent intégrer les profils de risque spécifiques à chaque agent dans un cadre global d’effet de classe pour les macroprogestatifs, et réévaluer les recommandations pour les microprogestatifs à mesure que des études comparatives de meilleure qualité deviennent disponibles.
Introduction
Les méningiomes sont les tumeurs primaires les plus courantes du système nerveux central chez les adultes, représentant environ 40 % des cas, avec une incidence de 9,5 pour 100 000 personnes-années. La plupart des méningiomes sont bénins et se développent lentement. Ils peuvent être détectés de manière fortuite ou se manifester par des symptômes neurologiques tels que des convulsions, des déficits focaux, des troubles neurocognitifs ou des maux de tête. Leur incidence est plus élevée chez les femmes, avec un rapport hommes/femmes de 2:1 après la puberté, qui passe à 3:1 pendant les années de reproduction. La progestérone joue un rôle important dans la physiopathologie des méningiomes : une augmentation de la taille des méningiomes a été signalée pendant la grossesse en raison de l’élévation des taux de progestérone, et des études ont documenté une prévalence de 38 à 88 % des récepteurs de progestérone dans les cellules des méningiomes. Les rapports faisant état de méningiomes intracrâniens chez des patientes traitées par des doses élevées d’acétate de cyprotérone (CPA) et d’autres progestatifs puissants ont suscité des inquiétudes quant à un lien de causalité potentiel et ont donné lieu à des études épidémiologiques spécialement conçues. Les progestatifs sont prescrits dans le monde entier à la fois pour des indications autorisées (par exemple, contraception, endométriose et hormonothérapie transgenre) et pour des utilisations non autorisées (par exemple, acné et alopécie féminine). L’acétate de médroxyprogestérone (DMPA) est l’un des contraceptifs injectables les plus utilisés dans le monde, en particulier dans les programmes de planification familiale à grande échelle, ce qui entraîne une exposition prolongée chez des millions de femmes. Des études de cohorte à grande échelle ont exploré le lien entre l’exposition aux progestatifs et le risque de méningiome, fournissant des données significatives ayant des implications socio-économiques, compte tenu de l’utilisation répandue des progestatifs. Les méningiomes étant des tumeurs à croissance lente, tout effet causal des progestatifs devrait se manifester principalement après une exposition cumulative à long terme ou élevée, tandis que les traitements à court terme sont peu susceptibles d’avoir une incidence significative sur le risque. Cette revue systématique et cette méta-analyse résument les connaissances actuelles sur les relations entre les méningiomes et les progestatifs, en mettant particulièrement l’accent sur les implications cliniques, avec une attention particulière portée à la dose, à la voie d’administration, à la durée d’exposition et aux implications cliniques pour la prise en charge des patients.
Méthodes
Stratégie de recherche et critères de sélection
Cette revue systématique a été réalisée et rapportée conformément aux lignes directrices MOOSE et à la déclaration PRISMA, suivant les recommandations méthodologiques récentes pour les méta-analyses en neurochirurgie. L’étude a été examinée et approuvée par un comité d’éthique institutionnel (IRB00011687, IRB #1 : 2024/53).
Le logiciel EPPI Reviewer (v.6.15) a été utilisé pour la sélection et le tri des études. Depuis la création de la base de données jusqu’au 1er novembre 2025, nous avons effectué des recherches dans la Bibliothèque nationale de médecine des États-Unis (PubMed/MEDLINE), Embase (OVID), la Bibliothèque Cochrane et la base de données EPI-PHARE afin d’identifier toutes les études épidémiologiques examinant les associations entre les méningiomes intracrâniens et l’exposition systémique aux progestatifs. Les enregistrements en double ont été identifiés et supprimés. Les titres et les résumés des études ont été examinés par rapport aux critères d’inclusion. Les études en texte intégral ont été importées et évaluées en vue de leur inclusion. En outre, nous avons utilisé un « backward snowballing» et examiné les rapports de pharmacovigilance et les directives réglementaires nationales/internationales (y compris celles de l’EMA et des agences nationales). Le premier auteur (B.H.) a examiné les titres/résumés ; l’auteur principal (J.P.) a examiné les textes intégraux et validé les exclusions basées sur les résumés ; les désaccords ont été résolus par consensus ou, si nécessaire, par un troisième évaluateur (A.R.).
Les publications étaient éligibles si elles répondaient aux critères suivants : (1) articles complets rédigés en anglais ou en français ; (2) rapportant une association entre l’exposition aux progestatifs et les méningiomes ; (3) localisation intracrânienne du méningiome. Les progestatifs systémiques administrés par voie orale, par injection ou par voie intra-utérine étaient éligibles ; les préparations purement locales ou topiques sans absorption systémique significative ont été exclues. Seules les études épidémiologiques (transversales, cas-témoins, cohortes) utilisant des méthodes basées sur les données ont été incluses dans la méta-analyse. Les rapports transversaux descriptifs, les séries de cas de pharmacovigilance et les études expérimentales ont été résumés de manière narrative lorsqu’ils étaient pertinents, mais n’ont pas été regroupés.
À l’aide d’un formulaire standardisé, nous avons extrait les données relatives aux caractéristiques de l’étude (pays, année, conception et nombre de cas), au sexe (tel que rapporté dans les articles originaux) et aux caractéristiques d’imagerie (volume de la tumeur, évolution dans le temps, localisation). Pour les progestatifs, nous avons recueilli les caractéristiques (type, dose, durée et risque de méningiomes) et la voie d’administration (orale, injectable, intra-utérine). Nous avons utilisé l’échelle de Newcastle-Ottawa (NOS) pour évaluer la qualité méthodologique des études non randomisées. Cette échelle évalue la qualité dans trois domaines : (1) sélection des études (4 points), (2) comparabilité des groupes (2 points) et (3) exposition ou vérification des résultats (3 points). Les études obtenant un score de 7 points ou plus ont été classées comme étant de haute qualité. Deux évaluateurs (B.H. et J.P.) ont appliqué indépendamment l’échelle NOS et ont résolu les divergences en discutant avec un auteur senior (A.R.) lorsque cela était nécessaire. La certitude des preuves a été évaluée à l’aide de l’approche GRADE (Grading of Recommendations Assessment, Development and Evaluation). Les évaluations GRADE ont été réalisées au niveau de chaque contraste molécule-exposition entrant dans la synthèse quantitative, en partant d’une certitude « faible » pour les données observationnelles et en déclassant les risques de biais, d’incohérence, d’imprécision ou de biais de publication présumé, le cas échéant ; pour les expositions ayant des effets importants et cohérents et un gradient dose-réponse plausible, nous avons envisagé de les rehausser d’un niveau.
Lorsque plusieurs études évaluaient des expositions similaires sur la base de populations et de périodes susceptibles de se chevaucher, nous avons donné la priorité aux études de cohorte plutôt qu’aux études cas-témoins, en privilégiant celles qui comportaient des échantillons plus importants et des analyses dose-réponse plus solides. Cette stratégie visait à minimiser le risque de double comptage des individus et à préserver l’indépendance des estimations d’effet incluses dans la méta-analyse.
Analyse des données
Nous avons réalisé des méta-analyses à effets aléatoires sur l’échelle logarithmique des risques relatifs en utilisant une pondération générique par l’inverse de la variance et un estimateur du maximum de vraisemblance restreint pour τ2. Les estimations des effets ont été transformées en logarithmes avant d’être regroupées, puis retransformées pour être interprétées. L’hétérogénéité a été résumée par I2 et Tau.2 Les graphiques en forêt affichent les risques relatifs regroupés avec un IC à 95 %. Nous avons interprété I2 comme faible (<30 %), modéré (30-60 %), substantiel (60-90 %) et considérable (>90 %). Lorsque l’hétérogénéité était substantielle, nous avons également rapporté des intervalles de prédiction à 95 % et effectué des analyses d’influence « leave-one-out ». La synthèse quantitative a été limitée aux contrastes spécifiques à une molécule avec au moins deux études comparables. Toutes les analyses ont été réalisées à l’aide de R (v4.0.5) et des packages meta et metafor.
Nous avons prédéfini l’OR comme mesure de regroupement et avons effectué des méta-analyses sur l’échelle log-OR à l’aide de la méthode générique de l’inverse de la variance. Lorsque seuls le RR ou le HR étaient disponibles, nous avons utilisé les estimations ajustées rapportées sur l’échelle logarithmique et les avons traitées comme des approximations des OR, compte tenu de la faible incidence absolue des méningiomes intracrâniens.
Rôle de la source de financement
Cette étude n’a bénéficié d’aucune source de financement. Les auteurs ont eu pleinement accès à toutes les données incluses dans l’étude. BH et JP ont assumé la responsabilité finale de la décision de soumettre l’article pour publication.
Résultats
Le diagramme de flux PRISMA est présenté à la figure 1.
542 études ont été initialement identifiées : huit doublons ont été retirés, 436 ont été exclues sur la base du titre et du résumé, 12 n’ont pas été récupérées et huit ont été exclues sur la base du texte intégral. Au final, 78 études ont été incluses dans l’examen final. Parmi celles-ci, 14 études ont été jugées éligibles pour être incluses dans la méta-analyse (présentées dans le tableau 1), 5 étaient des études de cohorte et 9 étaient des études cas-témoins. Les 14 études ont toutes été classées comme étant de haute qualité selon le système de notation NOS ; cependant, même les études classées comme « de haute qualité » selon le NOS restaient sujettes à des facteurs de confusion résiduels et, dans certaines analyses basées sur des registres, à une classification erronée des résultats. Selon le système GRADE, la certitude des preuves était modérée pour la CPA à forte dose et faible pour le DMPA, et faible à très faible pour les autres progestatifs (reflétant la conception observationnelle, les facteurs de confusion résiduels, l’hétérogénéité et l’imprécision pour plusieurs expositions).
Caractéristiques des études incluses.
CPA : acétate de cyprotérone ; NOMAC : acétate de nomégestrol ; CMA : acétate de chlormadinone ; DMPA : acétate de médroxyprogestérone injectable.
La classification des progestatifs synthétiques, leurs modes d’action, leurs indications et leurs posologies sont résumés dans le tableau 2.
Tableau 2
Résumé des données probantes sur le risque de méningiome intracrânien associé aux progestatifs.
∗Utilisation restreinte/surveillée dans plusieurs pays en raison du risque de méningiome (spécifique à la classe/molécule).
†Les contextes varient selon les pays et peuvent être hors AMM.
%Présenté en OR combiné (CPA et DMPA) ou en OR.
∗∗Des notes de certitude GRADE ont été attribuées aux expositions pour lesquelles il existait des données épidémiologiques comparatives suffisantes ; pour les autres expositions, les données étaient insuffisantes pour étayer une évaluation GRADE.
THS : traitement hormonal substitutif ; SPM : syndrome prémenstruel ; SAU : saignements utérins anormaux.[BH1]
Risque de méningiome
Acétate de cyprotérone (CPA)
Le CPA est le premier progestatif identifié en 2007 comme pouvant être associé à des méningiomes. Depuis, des rapports de cas et des études de cohorte portant ont documenté la survenue de méningiomes dans le contexte d’une exposition au CPA. Toutes les études convergent vers une association claire entre des doses élevées ou une accumulation élevée de CPA. Gil et al. ont constaté en 2011 une augmentation du risque de méningiome chez les personnes utilisant des doses élevées de CPA (aRR : 11,4, IC à 95 % : 4,3-30,8), avec 4 cas sur 2 474 personnes exposées au CPA par rapport aux personnes non exposées au CPA. Cea-Soriano et al. ont identifié en 2012 un risque accru de méningiome associé à une exposition à des doses élevées de CPA (OR : 6,30, IC à 95 % : 1,4-28,9 ; 3 cas), mais pas à des doses faibles. L’exposition à des doses élevées de CPA concernait presque exclusivement les hommes, tandis que l’exposition à des doses faibles de CPA dans les contraceptifs oraux combinés concernait les femmes. Une vaste étude de cohorte française menée par Weill et al. en 2021 a identifié un risque de méningiome chez les patients exposés au CPA (HR : 6,6, IC à 95 % : 4,0-11,1 ; 69 cas). Ils ont observé une relation dose-réponse avec un risque plus élevé pour une dose cumulative élevée de CPA (> 60 g ; HR : 21,7, IC à 95 % : 10,8-43,5 ; 15 cas). Il est à noter qu’un an après l’arrêt de l’exposition au CPA, le risque de méningiome restait plus élevé dans le groupe exposé que dans le groupe non exposé (HR : 1,8, IC à 95 % : 1,0-3,2 ; 34 cas). Une étude française ultérieure menée par Hoisnard et al. en 2022 a confirmé le risque de méningiome lié à l’exposition au CPA (OR : 18,3, 16,0-21,1 ; 961 cas). Ils ont observé l’association la plus forte avec une exposition au CPA > 1 an (OR : 22,7, IC à 95 % : 19,5-26,6 ; 931 cas). Une étude de cohorte danoise menée par Mikkelsen et al.60 en 2022 a confirmé l’association dose-dépendante entre l’exposition au CPA et le risque de méningiome (exposition cumulative au CPA de 0,1 à 10 g, HR : 7,0, IC à 95 % : 3,1-15,6, 6 cas/exposition cumulative > 10 g, HR : 19,2, IC à 95 % : 10,3-35,8, 10 cas).Une méta-analyse précédente réalisée par Lee et al. a tenté de regrouper les données sur les progestatifs et les méningiomes, mais elle contenait plusieurs inexactitudes numériques (par exemple, des tailles d’échantillon erronées dans les principales études de registre et un traitement incohérent du temps-personne) et a rapporté une association non significative entre l’utilisation de CPA et le risque de méningiome (RR : 3,78, IC à 95 % : 0,31-46,39). Compte tenu de ces problèmes méthodologiques, nous ne nous sommes pas appuyés sur leurs estimations regroupées et avons plutôt présenté une synthèse indépendante basée sur une nouvelle extraction et une nouvelle analyse des études originales. Plusieurs recherches ont porté uniquement sur de faibles doses de CPA, et aucune d’entre elles n’a trouvé de lien avec le méningiome, même en cas d’utilisation à long terme. Le rapport récent du groupe d’intérêt scientifique EPI-PHARE de l’Agence nationale française de sécurité du médicament et des produits de santé, rédigé par Roland et al. en 2023 a confirmé le lien significatif entre l’exposition au CPA et le risque de méningiome (OR : 19,21, IC à 95 % : 16,61-22,22 ; 891 cas).
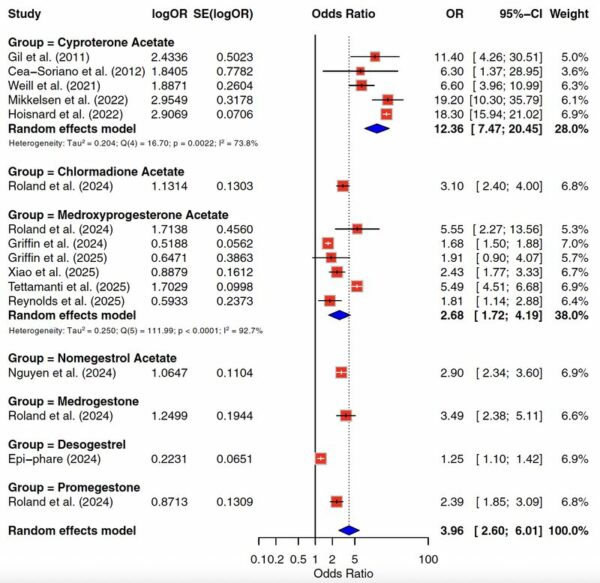
Après conversion du HR/RR en OR et restriction de l’analyse à une exposition à des doses élevées ou cumulées élevées de CPA, l’OR combiné était de 12,36 (IC à 95 % : 7,47-20,45), avec une hétérogénéité importante (I2 = 73,8 %, τ2 = 0,204 ; n = 5 études, 1047 cas). Les analyses « leave-one-out » n’ont pas changé la direction. Les études évaluant le risque de méningiome lié à l’utilisation de CPA sont résumées dans la figure 2 et le tableau 3.
Tableau 3
Résumé des risques relatifs combinés pour l’exposition aux progestatifs avec méta-analyses formelles.
Les participants fournissant des données font référence au nombre de cas de méningiome (événements) parmi les participants exposés contribuant à l’estimation combinée ; la taille totale des cohortes n’a pas été rapportée de manière cohérente dans toutes les études.
Acétate de chlormadinone (CMA)
Le lien potentiel entre la CMA et les méningiomes a été signalé pour la première fois par Shimizu et al. en 2008. En 2020, Roux et al. ont rapporté un autre cas de diminution du volume d’un méningiome après l’arrêt de la CMA, suggérant encore davantage un lien possible. En 2021-2022, Malaize et al. Graillon et al. Devalckeneer et al. et Samoyeau et al. ont rapporté une stabilisation ou une régression des méningiomes après l’arrêt du CMA. Avant 2022, Grandi et al. mettaient en garde contre toute conclusion définitive en raison du nombre limité de données disponibles. Une étude épidémiologique menée par le groupe d’intérêt scientifique EPI-PHARE par Hoisnard et al. en 2022 a identifié un risque significatif de méningiomes en cas d’exposition au CMA (OR : 4,7, IC à 95 % : 4,5-5,3 ; 683 cas). Un rapport de cohorte EPI-PHARE SNDS (Système national des données de santé) publié en 2021 a identifié pour la première fois un risque accru de méningiome en cas d’exposition prolongée à des doses élevées de CMA, ce qui a ensuite été confirmé dans la mise à jour évaluée par des pairs de Roland et al. en 2024 (RR ajusté en fonction de l’âge : 3,1, IC à 95 % : 2,4-4,0 ; 164 cas). Dans le groupe le plus exposé (dose cumulative) (> 8,64 g), le RR ajusté en fonction de l’âge de développer un méningiome était de 6,9 (IC à 95 % : 5,1-9,2 ; 86 cas) par rapport au groupe témoin, ce qui suggère un effet dose-réponse. Le rapport le plus récent du groupe d’intérêt scientifique EPI-PHARE a confirmé l’association significative entre l’exposition aux CMA et le risque de méningiomes (OR : 3,87, IC à 95 % : 3,48-4,30 ; 628 cas).
Compte tenu du nombre limité et de l’hétérogénéité des conceptions, nous n’avons pas effectué de méta-analyse groupée pour la CMA et fournissons une synthèse narrative (résumée dans la figure 2).
Acétate de médroxyprogestérone (MPA)
L’association potentielle entre le MPA et les méningiomes a été évaluée pour la première fois par Korhonen et al. en 2012 et n’a pas permis d’identifier un risque accru. Les limites de l’étude comprenaient l’inclusion de tous les progestatifs dans le même groupe et la restriction à l’exposition à un traitement hormonal substitutif postménopausique uniquement. Abou-Al-Shaar et al. ont été les premiers à suggérer, en 2023, l’association entre l’utilisation du MPA et le risque de méningiome. Pourhadi et al. ont mené en 2023 une étude épidémiologique au Danemark sur le traitement hormonal postménopausique et les méningiomes sans analyse spécifique de la MPA. Ils ont rapporté un risque plus élevé à la fois dans le groupe œstrogène-progestatif (HR : 1,21, IC à 95 % : 1,06-1,37 ; 423 cas) et dans le groupe sous progestatif seul (HR : 1,28, IC à 95 % : 1,05-1,54 ; 143 cas), suggérant une association potentielle entre le traitement hormonal de la ménopause contenant des progestatifs, largement basé sur la MPA dans ce contexte, et le méningiome.
Une étude cas-témoins basée sur le registre américain de Griffin et al. en 2024 a suggéré que l’exposition orale à la MPA n’était pas associée à un risque accru de méningiome, contrairement à l’exposition à la DMPA (OR : 1,68, IC à 95 % : 1,50-1,87 ; 480 cas), et que le risque augmentait avec la durée d’exposition (exposition ≤ 1 an, OR : 1,23, IC à 95 % : 1,10-1,38 ; 457 cas, et exposition > 3 ans, OR : 2,50, IC à 95 % : 2,06-3,04 ; 170 cas). Le rapport 2024 du groupe d’intérêt scientifique EPI-PHARE a fait état d’une association significative entre l’exposition au DMPA et les méningiomes en France (OR : 5,55, IC à 95 % : 2,27-13,56 ; 9 cas). Plus récemment, en 2025, plusieurs études à grande échelle menées auprès de la population et portant spécifiquement sur le DMPA ont confirmé ce signal : Xiao et al. ont constaté, en 2025, un risque accru de méningiome chez les personnes utilisant le DMPA (RR : 2,43, IC à 95 % : 1,77-3,33 ; 131 cas), Reynolds et al. ont rapporté dans une étude cas-témoins imbriquée un risque élevé associé à l’« utilisation à tout moment » du DMPA (OR : 1,81, IC à 95 % : 1,14-2,89 ; 29 cas), avec des estimations nettement plus élevées pour une exposition prolongée et un risque supplémentaire faible ou nul pour une utilisation à court terme.Tettamanti et al. ont observé, dans une étude cas-témoins menée à l’échelle nationale en Suède, une forte association entre le DMPA et le méningiome (RC : 5,49, IC à 95 % : 4,51-6,67 ; 186 cas). En outre, une étude cas-témoins américaine plus récente, menée par Griffin et al.76 à l’aide de comparateurs hormonaux actifs et non actifs, a rapporté un risque excessif non significatif mais cohérent dans le sens d’une exposition antérieure au DMPA (OR : 1,91, IC à 95 % : 0,99-4,50 ; 7 cas), ce qui renforce l’hypothèse d’un effet de classe possible du DMPA. Dans l’ensemble, ces données convergentes indiquent que le risque supplémentaire est largement dû à une exposition prolongée ou répétée au DMPA, tandis que le MPA oral et les traitements de courte durée ne montrent pas d’association cohérente avec le méningiome.
L’OR combiné, limité au DMPA, était de 2,68 (IC à 95 % : 1,72-4,19), avec une hétérogénéité importante (I2 = 92,7 %, τ2 = 0,25 ; n = 6 études, 842 cas exposés). Les analyses « leave-one-out » n’ont pas changé la direction. Les études évaluant le risque de méningiome lié à l’utilisation de la MPA sont résumées dans la figure 2 et le tableau 3.
En revanche, les études évaluant la MPA par voie orale, principalement dans le cadre d’un traitement hormonal de la ménopause ou d’un traitement oral à base de progestatif seul, n’ont généralement rapporté aucune augmentation ou seulement une augmentation modeste du risque de méningiome. Dans l’ensemble, ces résultats confirment que tout risque potentiel lié à la MPA par voie orale est probablement nettement inférieur à celui observé avec le DMPA à effet retard, et peut se limiter à une utilisation continue à long terme dans des populations spécifiques.
Acétate de nomégestrol (NOMAC)
Le lien potentiel entre le NOMAC et le méningiome a été signalé pour la première fois par Gruber et al. en 2004. Gruber et al. ont rapporté en 2011 quatre cas de patients chez lesquels un méningiome avait été diagnostiqué pendant un traitement par NOMAC, et aucun n’a présenté de signes de récidive après la chirurgie et l’arrêt du NOMAC. Sept autres rapports de cas ont décrit des cas similaires de méningiome chez des patients traités par NOMAC20, et de nombreuses études ont été publiées sur des patients atteints de méningiome exposés au NOMAC. Entre 2021 et 2022, Samarut et al. Malaize et al. Graillon et al. Devalckeneer et al.42 et Samoyeau et al.34 ont suggéré un lien entre l’utilisation du NOMAC et le méningiome. Cependant, la petite taille des échantillons (comprenant entre 1 et 12 patients) n’a pas permis d’établir un lien définitif.
Une étude épidémiologique menée par le groupe d’intérêt scientifique EPI-PHARE a identifié un risque significatif de développer un méningiome chez les patients exposés au NOMAC (OR : 4,7, IC à 95 % : 4,3-5,1 ; 969 cas). L’EPI-PHARE a d’abord signalé une augmentation du risque de méningiome en cas d’exposition prolongée/à forte dose au NOMAC dans une étude SNDS de 2021, confirmée et développée par la suite dans une analyse actualisée en 2024 (RR ajusté en fonction de l’âge : 2,9, IC à 95 % : 2,4-3,7 ; 171 cas), avec un gradient dose-réponse marqué (RR 12,0 pour une exposition cumulative > 6 g). Le dernier rapport du groupe d’intérêt scientifique EPI-PHARE publié en 2024 a fait état d’une association significative entre l’exposition au NOMAC et les méningiomes (OR : 4,93, IC à 95 % : 4,50-5,41 ; 925 cas).
Compte tenu du nombre limité et de l’hétérogénéité des conceptions, nous n’avons pas effectué de méta-analyse groupée et fournissons une synthèse narrative (résumée dans la figure 2).
Promégestone
Abijaoude et al. ont rapporté en 2021 un cas unique d’ostéoméningiome apparu pendant un traitement à la promégestone. Apra et al. en 2020 et Graillon et al.41 en 2021 ont rapporté des séries de cas où des méningiomes ont été observés en concomitance avec un traitement à la promégestone, suggérant une association potentielle. Le rapport récent du groupe d’intérêt scientifique EPI-PHARE69,86 a identifié un risque significatif de développer un méningiome chez les patients exposés à la promégestone (OR : 2,39, IC à 95 % : 1,85-3,09 ; 83 cas). L’utilisation prolongée de promégestone pendant ≥ 1 an était associée à un risque plus élevé (OR : 2,74, IC à 95 % : 2,04-3,67 ; 66 cas).
Compte tenu du nombre limité et de l’hétérogénéité des conceptions, nous n’avons pas effectué de méta-analyse groupée et fournissons une synthèse narrative (résumée dans la figure 2).
Médrogestone
L’association potentielle entre la médrogestone et les méningiomes a été suggérée pour la première fois par Apra et al. en 2020. Le rapport du groupe d’intérêt scientifique EPI-PHARE de Roland et al. a identifié un risque significatif de développer un méningiome chez les patients exposés à la médrogestone (OR : 3,49, IC à 95 % : 2,38-5,10 ; 42 cas). L’utilisation prolongée de médrogestone pendant ≥ 1 an était associée à un risque plus élevé (OR : 4,08, IC à 95 % : 2,72-6,10 ; 40 cas).
Compte tenu du nombre limité et de l’hétérogénéité des conceptions, nous n’avons pas effectué de méta-analyse groupée et fournissons une synthèse narrative (résumée dans la figure 2).
Désogestrel
Le lien entre le désogestrel et les méningiomes a été étudié pour la première fois dans le récent rapport du groupe d’intérêt scientifique EPI-PHARE. Ce dernier a identifié un risque significatif de développer un méningiome chez les patientes exposées au désogestrel (RC : 1,25, IC à 95 % : 1,10-1,42 ; 287 cas). Le risque apparaît après cinq ans d’utilisation du désogestrel (OR : 1,70, IC à 95 % : 1,39-2,08 ; 115 cas) et augmente avec la durée d’exposition au désogestrel (5-6 ans d’utilisation, OR : 1,51, IC à 95 % : 1,17-1,94 ; 71 cas, et ≥ 7 ans d’utilisation, OR : 2,09, IC à 95 % : 1,51-2,90, 44 cas). Si le désogestrel a été arrêté depuis plus d’un an, le risque de développer un méningiome disparaissait (OR : 0,83, IC à 95 % : 0,63-1,09 ; 58 cas). S’appuyant sur ces données, Roland et al. ont publié en 2025 une vaste étude cas-témoins nationale, basée sur la même cohorte, et ont démontré qu’une utilisation prolongée (≥ 5 ans) de 75 μg de désogestrel était associée à un risque accru de méningiome intracrânien (OR : 1,70, IC à 95 % : 1,39-2,08, 115 cas), avec une association plus forte pour une utilisation ≥ 7 ans (OR : 2,09, IC à 95 % : 1,51-2,90, 44 cas).
Compte tenu du nombre limité et de l’hétérogénéité des conceptions, nous n’avons pas effectué de méta-analyse groupée et fournissons une synthèse narrative (résumée dans la figure 2).
Autres progestatifs
Plusieurs études ont exploré l’association entre d’autres progestatifs (notamment la dydrogestérone, le lévonorgestrel, la noréthistérone, la progestérone, l’hydroxyprogestérone, la spironolactone et le diénogest) et les méningiomes.
Aucune d’entre elles n’a identifié de lien clair. Le groupe d’intérêt scientifique EPI-PHARE a étudié l’utilisation des progestatifs largement prescrits en France entre 2009 et 2018. Il n’a trouvé aucune association significative entre un risque accru de chirurgie pour méningiome intracrânien et l’exposition à la progestérone orale ou intravaginale (OR : 0,88 (IC à 95 % : 0,78-0,99) ; 329 cas), la progestérone percutanée (OR : 1,11 (IC à 95 % : 0,89-1,40) ; 90 cas), la dydrogestérone (OR : 0,96 (IC à 95 % : 0,81-1,14) ; 156 cas), spironolactone (OR : 0,95 (IC à 95 % : 0,84-1,09) ; 264 cas), diénogest (OR : 1,48 (IC à 95 % : 0,41-5,35) ; 3 cas), système intra-utérin à 52 mg de lévonorgestrel (OR : 0,94 (IC à 95 % : 0,86-1,04) ; 566 cas) et système intra-utérin à 13,5 mg de lévonorgestrel (OR : 1,39 (IC à 95 % : 0,70-2,77) ; 10 cas). Aucun cas d’exposition à l’hydroxyprogestérone n’a été trouvé. Cependant, le groupe d’intérêt scientifique EPI-PHARE a souligné qu’aucune conclusion ne pouvait être tirée concernant le diénogest ou l’hydroxyprogestérone en raison du petit nombre de personnes recevant ces médicaments.
Compte tenu du nombre limité et de l’hétérogénéité des conceptions, nous n’avons pas effectué de méta-analyse groupée et fournissons une synthèse narrative (résumée dans la figure 3).
Fig. 3 Progestatifs non associés à un risque accru de méningiomes.
Risque de méningiome malin
Les méningiomes malins de grade 3 selon la classification de l’OMS sont rares, représentant 1 à 2 % des cas.1 Comme l’ont rapporté Roux et al. en 2022, des cas de méningiomes malins ont été observés en association avec des progestatifs, ce qui suggère un risque potentiellement plus élevé lié à ces médicaments. Le groupe d’intérêt scientifique EPI-PHARE³⁹ a démontré que l’exposition aux progestatifs était associée à une augmentation significative du risque de méningiomes malins chez les femmes pour le CPA (OR : 23,7, IC à 95 % : 8,1-69,8 ; 20 cas), le NOMAC (OR : 4,9, IC à 95 % : 2,2-10,8 ; 13 cas) et CMA (OR : 2,8, IC à 95 % : 1,3-5,9 ; 11 cas). Ces résultats ont été confirmés par Roland et al. en 2024, qui ont signalé une augmentation significative du risque de méningiomes malins pour le CPA (OR : 22,5, IC à 95 % : 7,61-66,48 ; 18 cas), NOMAC (OR : 4,95, IC à 95 % : 2,29-10,68 ; 13 cas) et CMA (OR : 5,78, IC à 95 % : 2,39-14,00 ; 11 cas). Aucun méningiome malin n’a été observé chez les cas exposés à la médrogestone, à l’acétate de médroxyprogestérone ou à la promégestone.
Croissance des méningiomes
Les effets du sevrage médicamenteux sur la croissance spontanée des méningiomes non traités ont été rapportés dans 16 études pour le CPA (allant de 1 à 188 cas), dans 10 études pour le NOMAC (variant de 1 à 6 cas), dans sept études pour le CMA (un cas par étude), dans une étude pour le MPA70 (10 cas) et dans deux études pour la promégestone (un cas par étude). Aucune étude n’a été identifiée pour les autres progestatifs.
Pour le CPA, l’arrêt du traitement entraîne une réduction significative de la tumeur à l’IRM : régression dans 36 à 92 % des cas, stabilité dans 8 à 85,2 % des cas, et croissance continue dans 0 à 29 % des cas.42 La plupart des études portaient sur divers progestatifs et examinaient les variations de volume chez toutes les patientes exposées aux progestatifs, ce qui rend difficile de tirer des conclusions pour chacun d’entre eux : régression dans 0 à 12,5 % des cas, stabilité dans 60,0 à 62,5 % des cas et croissance continue dans 25,0 à 40,0 % des cas pour le NOMAC³⁸ ; aucune régression, stabilité dans 66,7 % des cas et croissance continue dans 33,3 % des cas pour le CMA.38 Graillon et al. ont combiné les données du CMA et du NOMAC (11 cas au total) et ont constaté une régression dans 18 % des cas, une stabilité dans 64 % des cas et une croissance continue dans 18 % des cas.
Abou-Al-Shaar et al. ont suivi 10 femmes après l’arrêt du MPA : chez cinq d’entre elles, les tumeurs ont régressé ; chez trois autres, le DMPA avait été arrêté moins d’un an auparavant, ce qui empêchait de tirer des conclusions définitives ; deux ont été perdues de vue. Graillon et al. et Abi Jaoude et al. ont chacun rapporté un seul cas de régression d’un méningiome après l’arrêt du promégestone. Une illustration est présentée dans les données supplémentaires.
L’évolution des ostéoméningiomes après l’arrêt du progestatif reste incertaine. Des rapports suggèrent que la composante durale des méningiomes a régressé et que la composante osseuse a continué à croître et a même présenté un taux de croissance accru après l’arrêt du progestatif.
Localisation de la tumeur
Les séries publiées ont rapporté une localisation prédominante des méningiomes à la base antérieure et moyenne du crâne, quel que soit le progestatif utilisé, comme le résument la figure 4. Cela contraste avec la localisation prédominante des méningiomes au niveau de la convexité crânienne dans la population générale.
Dans les sept plus grandes études épidémiologiques, quel que soit le progestatif spécifique examiné, la base antérieure du crâne variait de 20 à 37 % et la base moyenne du crâne de 20 à 39 %. En revanche, bien que la convexité crânienne soit le site le plus fréquent dans la population générale, aucune de ces études n’a rapporté un taux de localisation de la convexité supérieur à celui de la base antérieure ou moyenne du crâne.
Fig. 4 Localisation des tumeurs. La localisation des tumeurs, quel que soit le progestatif, est classée comme convexité (A.), base crânienne moyenne (B.) et base crânienne antérieure (C.), représentées respectivement en bleu, vert et violet.





